코로나 19 팬데믹의 장기화로 인해 임상 환자 모집 등의 어려움을
겪거나 연구가 중단·지연되는 일이 빈번하게 일어남에도 불구하고, 알츠하이머병
치료제 개발 영역에는 여전히 다양한 연구들이 시도되고 있다.
한국바이오협회 바이오경제연구센터는 '알츠하이머의 진단과 치료 동향' 브리프를 발간했다. 재생의료연합(ARM)에서
발간한 자료를 바탕으로, 알츠하이머 진단 및 바이오마커 개발동향, 신약
파이프라인 분석, 국내 치료제 개발 동향을 분석했다.
2022년 1월 5일 기준, 미국국립보건원 운영 임상시험정보사이트에서 발표된 알츠하이머
신약 파이프라인 연례보고서에 따르면, 전 세계에서 143개
신약 후보물질을 대상으로 총 172건의 임상시험이 시행됐다.
상용화에 가장 근접한 임상 3상에 진입한 신약 후보물질은 31개 (임상 47건)로, 임상 2상 82개 (임상 94건), 임상 1상은 30개(임상 31건)로 연구가
진행됐다.
세부적으로, 원인조절치료제(Disease-modifying
therapy, DMT)는 143개의 전체 후보 물질 중 119개 (83.2%)로 대부분을 차지했다.
2021년 신약 임상에서도 DMT의
경우, 126개 전체 후보물질 가운데 104개를 차지하며 82.5%의 높은 점유율을 보인만큼, 해당 용도의 후보물질은 꾸준히
큰 비중을 차지하고 있다. 다음으로 인지기능 강화제 14개(9.8%), 신경정신행동 증상 개선제가 10개(6.9%)로 나타났다.
원인조절치료제의 종류는 바이오의약품 40개(33.6%), 저분자 의약품 79개(66.4%)로
구분됐으며, 원인조절치료제 용도의 후보물질 임상은 아밀로이드 베타 표적 계열이 20개(16.8%), 타우 단백질 표적 계열이 13개(10.9%)로 나타났다.
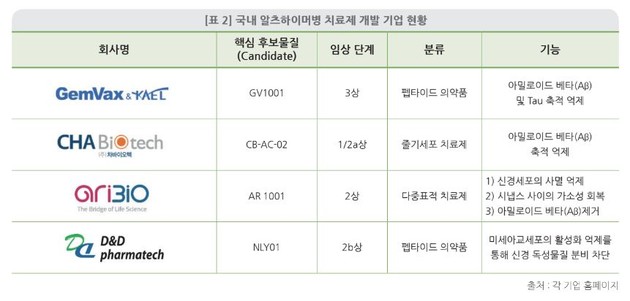
국내 바이오제약 기업의 경우에도 줄기세포 치료제, 펩타이드 의약품
등 알츠하이머병 치료제 개발 또한 활발하게 이뤄지고 있으며, 경구제나 주사제 이외에도 다양한 제형의
임상 및 상용화를 진행 중에 있다.
국내 바이오제약 기업의 줄기세포치료제, 펩타이드 의약품 등 알츠하이머병
치료제 개발 또한 활발히 이뤄지고 있다. 예로 들면, 젬백스앤카엘은
식약처로부터 중증 알츠하이머병 환자를 대상으로 펩타이드의약품에 해당되는 'GV1001' 에 대해 3상 임상시험을 승인받았다.
차바이오텍은 줄기세포 치료제 기반의 알츠하이머병 치료제를 개발 중이다. 아리바이오는
단일 기전 약물에 집중해 온 다국적 제약사들과는 다르게, 약물 하나로 여러 작용을 하는 '다중기작' 약물을 개발 중이다. 에이비엘
바이오는 바이오 항체 치매신약 개발을 진행 중이다.
이밖에도 셀트리온은 국내 경피용약물전달시스템 개발 기업 아이큐어와의 공동개발을 통해 알츠하이머병 치매 치료용
도네페질 패치제에 대한 식약처 품목허가를 획득했다. 관련 기업들은 경구제·주사제 이외에도 다양한 제형의 임상과 상용화를 진행하고 있다.
한국바이오협회 관계자는 "알츠하이머 치료제 신약 개발에 대한
성공확률이 낮은 만큼 향후 정부의 적극지원과 민간 투자가 중요할 것으로 보이며, 앞으로의 치료제는 '완화'의 개념이 아닌, 명확한
원인을 '치료'하는 개념으로 변화돼야 할 필요가 있을 것으로
보인다"고 밝혔다.