미충족 의료 수요가 큰 난치성 질환의 근본적 치료 대안으로 첨단바이오의약품이 떠오르고 있다. 특히 재생의료연합(Alliance for Regenerative Medicine)에서 지난 2021년 발표한 자료에 따르면, 오는 2027년까지 시장 규모가 504억 달러로 추정돼, 향후 주요 치료제 산업으로 자리매김할 전망이다.
한국바이오협회에서는 지난 3일 '재생의료 산업 및 임상 동향(첨단바이오의약품을 중심으로)'보고서를 발간했다. 차바이오텍 유지민 실장과 바이오경제연구센터 김지운 연구원은 보고서를 통해 첨단바이오의약품 신약 개발과 시장을 긍정적으로 전망했다.
첨단바이오의약품은 손상된 세포와 조직, 장기 등을 대체 및 복원하는 의약분야에 최근 발전한 혁신적 치료기술이 융합된 세포치료제, 유전자치료제, 조직공학치료제 등을 말한다.
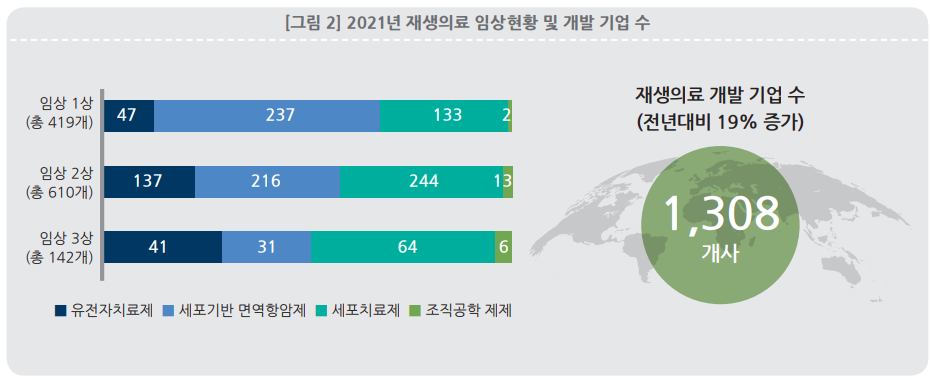
현재 전 세계적으로 활발한 연구개발이 진행 중이며, 재생의료연합에서 글로벌 임상시험 현황을 분석한 결과, 2021년 기준 1,171건의 임상시험이 이뤄지는 것으로 나타났다. 특히 이 중 142건(12%)은 임상 3상이 진행 중이었다. 미국 FDA와 유럽 EMA에서는 2025년까지 기관별 연 10건에서 최대 20건까지 세포유전자치료제가 승인될 것으로 예상했다.
임상시험 중인 치료제의 기전별로 살펴보면, 세포기반 면역항암제가 41% 비중을 차지해 가장 많은 것으로 나타났다. ▲세포기반 면역항암제 484건 ▲세포 치료제 441건 ▲유전자 치료제 225건 ▲조직 공학제제 21건으로 나타났다. 아울러 글로벌 재생의료 기업 수는 2021년 기준 총 1,308개로 집계됐다.
재생의료 시장의 성장은 선진국 규제기관에서 패스트트랙 제도 활성화를 통한 신속한 허가를 들 수 있다. 또 알츠하이머, 척추손상, 당뇨 등 적절한 치료방법이 없는 질환에서 새로운 패러다임을 가져오고 있기 때문으로 예측된다.
지난해 기준 미국, 유럽, 중국 등에서 6개의 재생의료 관련 신약이 승인됐다. 지난 2월에 Legend Biotech & Janssen의 다발성 골수종 대상 CAR-T 치료제인 CARVYKTI(ciltacabtagene autoleucel)가 추가로 승인됐다.

국내에서 허가받은 첨단바이오의약품은 총 18개 품목으로 나타났고, 셀로텍, 테고사이언스, 바이오솔루션, 지씨셀, 안트로젠, 에스바이오메딕스, 파미셀, 메디포스트, 바이오솔루션이 해당 품목을 보유한 것으로 나타났다.
김지운 연구원과 유지민 실장은 보고서를 통해 “전 세계적으로 초고령 사회로 진입함에 따라 퇴행성·난치성·만성질환이 급속도로 증가하고 있고, 고품질 의료기술에 대한 요구가 증가하며 첨단 의료기술 요구가 증대되고 있다”고 설명했다.
이어 “그러나 아직 첨단바이오의약품은 가격 경쟁력이 낮고, 신약에 대한 인허가에 어려움이 존재한다”라며 “단계적 절차를 통해 재생의료 치료제에 관한 임상연구의 안전성과 유효성, 급여등재까지 보장된다면, 향후 새로운 시장영역을 창출할 수 있는 산업으로 자리매김할 수 있을 것”이라고 전했다.